Điều trị ung thư ở những năm trước 1900
Ung thư được xem là một bệnh lý hiện đại, tuy nhiên gốc rễ của căn bệnh ung thư đã được hình thành từ trước đây rất lâu. Bằng chứng của ung thư được ghi nhận từ những tài liệu cổ xưa từ thời Ai Cập Cổ đại và nền Văn minh Hy Lạp 1. Cụ thể, vào năm 300 trước công nguyên (TCN), bằng chứng bằng chữ viết trên giấy cói (papyrus) đã ghi nhận một trường hợp ung thư vú và phẫu thuật điều trị đã được mô tả 2, 3. Vào năm 1500 TCN, di tích trên giấy cói của Ebers, thông tin về một số loại ung thư như ung thư da, ung thư tử cung, ung thư dạ dày và ung thư đại trực tràng đã được ghi chép 4.
Vào năm 400 TCN, ung thư được nhận biết như một bệnh lý do nguyên nhân sinh học riêng biệt hơn là do các hiện tượng siêu nhiên. Hippocrates là nhà khoa học đầu tiên mô tả ung thư một cách khoa học. Ông đã cân nhắc khối u là một bệnh lý được gây ra do sự mất cân bằng giữa 4 yếu tố chính của cơ thể (i) máu, (ii) đờm, (iii) mật đen và (iv) mật vàng. Giả thiết này của Hippocrates đã được Galen – một nhà khoa học sống ở thành Rome vào khoảng năm 130 – 200 sau công nguyên (SCN) cải thiện bằng nhận định ung thư là bệnh lý không thể chữa lành và nguyên nhân là do sự biến đổi của mật đen. Hơn nữa, Galen cũng đã định ra chiến lược phẫu thuật đầu tiên cho việc điều trị ung thư.
Một vài bằng chứng khảo cổ đã cho thấy ung thư xuất hiện trên trái đất trước cả sự xuất hiện của con người. Ở một vài mẫu hóa thạch của khủng long và sinh vật tiền sử đã cho thấy bằng chứng của những khối u trong xương (có thể là sarcina xương hoặc ung thư di căn xương) 5, 6.
Từ thời Hy Lạp cổ đại và La Mã cổ đại cho đến thời hiện đại, giả thiết của Hippocrates và Galen vẫn luôn là giả thiết được công nhận nhiều nhất. Hơn nữa, từ thời các triều đại Ai Cập cho đến cuối thế kỷ 19, việc điều trị ung thư vẫn đa số dựa trên chế độ ăn lành mạnh, đốt và phẫu thuật đối với những khối u trên bề mặt. Những khối u sâu vẫn chưa được tiếp cận điều trị, đa số bệnh nhân được giảm đau bằng chiết xuất từ cây thuốc phiện.
Ung thư được xem là một bệnh lý hiện đại kể từ năm 1970. Lúc bấy giờ, các nhà khoa học bắt đầu những nghiên cứu đầu tiên về một số hợp chất có khả năng gây ung thư (chẳng hạn như thuốc lá hoặc muội than). Kể từ thế kỷ 16 cho đến cuối thể kỷ 19, đã có nhiều tiến bộ trong y khoa, phẫu thuật và các biện pháp can thiệp nhờ vào những khám phá quan trọng của nhiều nhà khoa học trong lĩnh vực ung thư về các khía cạnh giải phẫu, sinh học, dịch tễ và điều trị. Những tiến bộ này bắt đầu từ từ những khám phá của Paracelsus (1493 – 1541) khi đạt ra những câu hỏi về giả thiết của Hippocrates và Galen cho rằng khối u được hình thành do sự tích tụ của “muối” trong máu của, cho đến Percival Pott khám phá ra mối liên hệ giữa ung thư tinh hoàn và sự phơi nhiễm thường xuyên với muội than ở người làm nghề cạo ống khói (1714 – 1788), cho đến nhận định về nguồn gốc của khối u ở những tế bào bị biến đổi của Rudolf Virchow (1821 – 1902) và cho đến những bước tiến đầu tiên của con người trong xạ trị nhờ vào phát hiện của Maries Curie và Pierre Curie. Tuy nhiên, cũng có thể xem rằng nguồn gốc của xạ trị được xuất phát từ cuối thế kỷ 19 với phát hiện của Wilhelm Conrad Röntgen về x – ray.
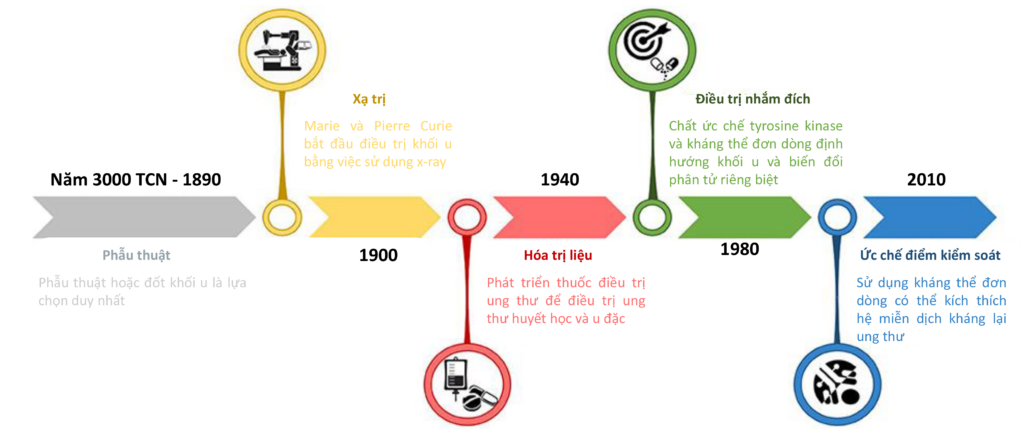
Mặc dù đã có nhiều phát hiện quan trọng trong lĩnh vực điều trị ung thư nhưng trước Chiến tranh Thế giới Lần thứ 2, cách tiếp cận điều trị ung thư vẫn đơn thuần nhằm loại bỏ căn nguyên và ngăn chặn khối u di căn. Do vậy, phẫu thuật vẫn luôn là lựa chọn duy nhất cho bệnh nhân ung thư vào thời bấy giờ bất chấp những tác động bất lợi của biện pháp này. Hình 1 tóm tắt những bước tiến quan trọng trong điều trị ung thư.

Hình 1. Tóm tắt chặng đường phát triển của điều trị ung thư
Sự ra đời và tiến bộ của hóa trị liệu trong điều trị ung thư
Sau sự khai phá và áp dụng của x – ray trong chẩn đoán và điều trị một số khối u, nghiên cứu và phát triển về những biện pháp điều trị mới trong lĩnh vực ung thư đã có một số sự ngưng trệ nhất định. Mãi cho đến những năm 40 của thế kỷ 20, một phát hiện lớn trong điều trị ung thư đã ra đời trong giai đoạn Chiến tranh Thế giới Lần thứ 2 – đó là sự phát hiện ra tác nhân alkyl hóa DNA (DNA alkylating agent) 7.
Tác nhân alkyl hóa
Tác nhân alkyl hóa đầu tiên (nitrogen mù tạt) được sử dụng cho mục đích lâm sàng là mechlorethamine, tác nhân này có khả năng gắn kết với nitrogen thứ 7 của guanine và ức chế sự nhân đôi của DNA. Tuy nhiên, những thế hệ nitrogen mù tạt đầu tiên không còn được sử dụng do độc tính cao và tế bào ung thư hình thành cơ chế đề kháng dược lý. Hiện nay, nitrogen mù tạt được sử dụng chủ yếu trong điều trị ung thư là cyclophosphamide.
Tác nhân alkyl hóa khác bao gồm carmustine, lomustine, semustin, streptozocin, nimustine, tallimustine, photemustine, một số alkyl sulfate như busulfan, treosulfan, mannosulfan, dẫn chất của ethyleneimine như thiotepa, triazichinone, epoxide như etoglucide, nhóm triazene như dacarbazine, temozolomide và một số muối kim loại như cisplatin, carboplatin, oxaliplatin và satraplatin. Trong số những hợp chất kể trên, dacarbazine và hợp chất của platinum là những tác nhân alkyl hóa vẫn được sử dụng rộng rãi như một lựa chọn đầu tay và lựa chọn hàng hai cho một số loại ung thư. Dacarbazin lần đầu tiên được tổng hợp bởi Shealy vào năm 1962 và được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ chấp thuận vào năm 1975 cho chỉ định điều trị ung thư hắc tố da và u lympho.
Nhóm chất ức chế chuyển hóa
Rất nhanh sau Chiến tranh Thế giới Lần 2, cách tiếp cận điều trị mới trong lĩnh vực ung thư đã được phát triển, dựa trên việc sử dụng những phân tử bắt chước cấu trúc của các chất chuyển hóa sinh lý. Chất ức chế chuyển hóa chính bao gồm folate analog, purine analog và pyrimidine analog.
Antifolate là thế hệ đầu tiên của nhóm chất ức chế chuyển hóa được nghiên cứu. Trong đó, aminopterin là chất folic acid analog đầu tiên có thể làm giảm sự sinh sôi của tế bào ung thư và phục hồi sự cân bằng nội môi của tủy xương 8. Trong số những dẫn chất nhóm antifolate được nghiên cứu, methotrexate là một trong những thuốc vẫn đang được sử dụng.
Trong những năm 50, nhiều hợp chất ức chế chuyển hóa khác được tổng hợp và vẫn được sử dụng cho đến hiện tại. Trong số đó, 6 – mercaptopurine và 5 – flourouracil vẫn được sử dụng nhiều trong thực hành lâm sàng ung thư.
Antimitotic có nguồn gốc tự nhiên
Tác nhân antimitotic đầu tiên được khai phá vào cuối những năm 50 được chiết xuất từ cây hoa dừa cạn (Catharanthus roseus) với tên Vinca alkaloid. Vinca alkaloid ban đầu được sử dụng để điều trị đái tháo đường, tuy nhiên, nghiên cứu của Noble và cộng sự đã cho thấy khả năng làm chậm sự tăng trưởng của khối u của hợp chất này. Do vậy, sau đó nhiều dẫn xuất của Vinca đã được tổng hợp. Trong số những hợp chất này, vinblastine, vincristine, vinorelbine, vindesine là những cấu trúc có hiệu quả điều trị lớn nhất.
Nhiều tác nhân antimitotic khác được chuyển hóa từ cây táo ma (Podophyllum peltatum), trong đó có podophyllin là hợp chất ban đầu được sử dụng để điều trị ung thư tế bào biểu mô và sarcomas. Những dẫn xuất khác của Podophyllum (epidodophyllotoxin) có thể làm ngưng quá trình tăng sinh của tế bào bằng việc chẹn topoisomerase II 9.
Nhóm tác nhân antimitotic bao gồm chất ức chế topoisomerase I (topotecan, irinotecan) và các phân tử ổn định vi ống, bao gồm taxane (paclitaxel, docetaxel, cabazitaxel). Kể từ năm 1996, irinotecan đã được chấp thuận cho chỉ định điều trị ung thư biểu mô đại trực tràng (đơn trị hoặc phối hợp với 5 – fluorouracil hoặc hợp chất chứa platinum), sau đó irinotecan cũng được sử dụng để điều trị ung thư phổi không tế bào nhỏ và ung thư buồng trứng 10.
Vào năm 1971, cấu trúc phân tủ của taxol đã được mô tả (antimiotic tự nhiên chiết xuât từ cây lá kim Taxus brevifolia. Tuy nhiên, cho đến 8 năm sau đó, Horwitz và cộng sự mới mô tả được cơ chế hoặc động của taxol. Có nhiều hoạt chất điều trị đã được chuyển hóa từ taxol, bao gồm paclitaxel, docetaxel (thế hệ tứ hai) và cabazitaxel (thế hệ thứ 3) đã được phát triển. Tất cả những hợp chất này là một cột mốc quan trọng trong điều trị nhiều loại u đặc bao gồm ung thư vú di căn, ung thư tụy (pancreatic adenocarcinoma), ung thư phổi không tế bào nhỏ, ung thư vùng đầu – cổ, ung thư dạ dày và ung thư tuyến tiền liệt.
Cytotoxic Antibiotic và hợp chất liên quan
Trong số những thuốc hóa trị liệu tiêu chuẩn, có một số kháng sinh và/hoặc dẫn xuất của kháng sinh có hoạt tính gây đọc tế bào, nhờ vậy, những hoạt chất này được sử dụng như một thuốc điều trị ung thư 11. Cơ chế hoạt động chủ yếu của nhóm chất này là tạo liên kết đồng hóa trị với acid nucleic và gây trở ngại cho quá trình tổng hợp DNA. Hợp chất đầu tiên được sử dụng của nhóm thuốc này là puromycin, tuy nhiên, puromycin không được sử dụng rộng rãi vì không chọn lọc và độc tính cao.
Vào năm 1960, daunomycin được phân lập từ chủng Streptomyces. Daunomycin có hiệu lực cao so với các hoạt chất các ở bệnh nhân tăng sinh lympho. Sau đó, vào năm 1968, một công thức mới được phân lập từ Streptomyces peucetius bị đột biến – adriamycin (doxorubicin). Hoạt chất này có hiệu lực cao trong điều trị ung thư ở chuột, tuy nhiên lại có độc tính cao đối với tim mạch.
Vào khoảng giữa những năm 50, hoạt chất actinomycin D được phân tập từ Streptomyces griseus. Cuối cùng, một hoạt chất kháng sinh điều trị ung thư khác được phân lập ở Nhật Bản vào 1966 vẫn được sử dụng cho đến ngày hôm nay – bleomycin.
Chất ức chế polyamine và chất điều biến sắt
Sự tăng sinh của tế bào và tăng trưởng của khối u được thúc đẩy bởi nhiều yếu tố, bao gồm cả polyamine. Do vậy, vào năm 1970, chất ức chế polyamine đầu tiên được tổng hợp và sử dụng trong thực hành lần đầu vào năm 1980.
Các thuốc điều trị ung thư khác được phát triển để điều biến nồng độ sắt nội bào. Sắt là nguyên tố vi lượng cốt lõi cho sự cân bằng nội môi của tế bào. Thiếu hụt sắt thường liên quan đến thiếu máu, trong khi dư thừa sắt dẫn đến stress oxy hóa ở mô, dẫn đến tình trạng viêm, rối loạn chức năng hệ thống và có thể dẫn đến những biến đổi về mặt di truyền. Do vậy, đã có nhiều nghiên cứu được tiến hành để phát triển các yểu tố điều biến sắt trong điều trị ung thư. Một số ví dụ cho nhóm hoạt chất này bao gồm desferrioxamine, di-2-pyridylketone-4,4,-dimethyl-3-thiosemicarbazone (Dp44mT), ciclopirox và triapine. Triapine là một trong những sắt chelate được sử dụng nhiều nhất trong điều trị ung thư trên lâm sàng để điều trị những khối u đặc.
Hóa trị liệu phối hợp trong điều trị ung thư
Trong những năm 60 và những năm 70, nhiều quy trình điều trị phối hợp sử dụng nhiều thuốc hóa trị liệu với nhiều cơ chế hoạt động hác nhau bắt đầu được đề nghị trong thực hành lâm sàng. Vào năm 1964, Vincent De Vita và cộng sự đã đề nghị phối hợp điều trị ung thư (cụ thể là Hodgkin’s lymphoma) lần đầu tiên. Phối hợp đầu tiên này có tên là MOPP (mechlorethamine – vincristine – procarbazine và prednisone). Phối hợp này đã đạ được nhiều kết quả quan trọng trong điều trị và trở thành một cột mốc quan trọng trong điều trị ung thư.
Trong những năm sau đó, kết quả nhiều nghiên cứu đã cho thấy hóa trị liệu có hiệu quả hơn trong việc điều trị những khối u nhỏ và khi được sử dụng phối hợp. Vào năm 1972, một phối hợp điều trị khác được đề xuất bởi Gianni Bonadonna và Umberto Veronesi, phối hợp này bao gồm cyclophosphamide, methotrexate và fluorouracil (CMF). Vào năm 1973, Bonadonna và nhóm cộng sự đã đề xuất phối hợp ABVD (adriamycine – belomycin – vinblastine – dacarbazine) trong điều trị Hodgkin’s lymphoma.
Sự phát triển của điều trị nhắm đích: chất ức chế chọn lọc kinase và kháng thể đơn dòng
Vào thời gian đầu của những năm 80, phát hiện mới trong lĩnh vực miễn dịch, sinh học tế bào và sinh học phân tử đã cho phép những nhà nghiên cứu khảo sát cơ chế phân tử liên quan đến sự phát triển của tế bào ung thư, từ đó xác định phân tử đích mới để chẹn bằng những hợp chất ức chế chọn lọc hoặc kháng thể đơn dòng. Nếu như những biện pháp hóa trị liệu tác động trên cả tế bào bình thường và tế bào ung thư, thì các biện pháp nhắm đích chỉ can thiệp trên những gen ung thị cốt lõi hoặc những gen ức chế sự tăng trưởng của khối u. Ngày nay, thuật ngữ trị liệu nhắm đích được dùng cho toàn bộ những biện pháp điều trị chỉ gây ảnh hưởng đến một phân tử đích cụ thể.
Vào năm 1980, Nadler và cộng sự đã điều trị bệnh nhân non-Hodgkin’s lymphoma (HDL) bằng kháng thể đơn dòng của chuột AB89, nhưng biện pháp điều trị này không gây ra những đáp ứng lâm sàng có ý nghĩa. Đây cũng là lần đầu tiên con người nỗ lực sử dụng kháng thể đơn dòng trong điều trị ung thư 12.
Cho đến những năm 90, những biện pháp điều trị nhắm đích mới cho thấy hiệu quả trong điều trị. Nhờ những nghiên cứu về genome của người và những tiến bộ trong kỹ thuật giải trình tự DNA, genomic, transcriptomic và proteomic, con người đã có những bước đột phá trong điều trị ung thư.
Ức chế điểm kiểm soát miễn dịch (Immune Checkpoint Inhibitor)
Miễn dịch trị liệu trong ung thư đã có nhiều bước tiến đáng kể trong những năm gần đây. Sau năm 2010, kháng thể đơn dòng mới định hướng kháng nguyên khối u hoặc thụ thể T-cell protein có thể giảm điều hòa đáp ứng miễn dịch đã được phát triển 13. Những biện pháp điều trị mới này được gọi là chất ức chế điểm kiểm soát miễn dịch và kháng thể đơn dòng anti-cytotoxic T-lymphocyte-associated antigen 4 và kháng kháng thể anti-programmed cell death protein 114.
Chất ức chế điểm kiểm soát miễn dịch đầu tiên được chấp thuận là ipilimumab vào năm 2011. Hiện nay, ipilimumab được sử dụng đơn trị hoặc phối hợp với nivolumab để điều trị ung thư tế bào hắc tố di căn hoặc không thể cắt bỏ.
Sau đó, 2 kháng thể đơn dòng ức chế điểm kiểm soát miễn dịch nivolumab và pembrolizumab được chấp thuận để điều trị ung thư phổi không tế bào nhỏ, ung thư tế bào hắc tố di căn, NHL và ung thư biểu mô đường tiết niệu khi những khối u vẫn còn dương tính với PD – L1. Vào năm 2018, durvalumab được chấp thuận để điều trị bệnh nhân mắc ung thư biểu mô đường tiết niệu di căn hoặc tiến triển.
Những chất ức chế điểm kiểm soát miễn dịch thường được sử dụng phối hợp với nhau hoặc phối hợp với nhóm thuốc hóa trị liệu khác15.
Bàn luận
Điều trị ung thư đã có nhiều bước tiến mang tính lịch sử, thuốc điều trị ung thư vẫn không ngừng được nghiên cứu và phát triển. Từ sau Chiến tranh Thế giới Lần 2 cho đến thời điểm hiện tại, những nhà nghiên cứu vẫn không ngừng đề xuất những biện pháp điều trị mới, cung cấp thêm lựa chọn cho bệnh nhân ung thư. Trong nhiều năm tới, sự phát triển và chấp thuận của nhiều thuốc hóa học, sinh học và công nghệ sinh học được mong chờ.
Tài liệu tham khảo
- Sudhakar, A. (2009). History of cancer, ancient and modern treatment methods. J. Cancer Sci. Ther. 1, 1–4. doi: 10.4172/1948-5956.100000e2
- Breasted, J. H. (1930). The Edwin Smith Surgical Papyrus. Chicago, IL: University of Chicago Press.
- Sanchez, G. M., and Meltzer, E. S. (2012). The Edwin Smith Papyrus: Updated Translation of the Trauma Treatise and Modern Medical Commentaries. Atlanta, GA: Lockwood Press.
- Kelly, J., and Mahalingam, S. (2015). Surgical treatment of head and neck cancers in the ancient world. J. Laryngol. Otol. 129, 535–539. doi: 10.1017/S0022215115001218
- Rothschild, B. M., Tanke, D. H., Helbling, M., and Martin, L. D. (2003). Epidemiologic study of tumors in dinosaurs. Naturwissenschaften 90, 495–500. doi: 10.1007/s00114-003-0473-9
- Dumbravbrevea, M. D., Rothschild, B. M., Weishampel, D. B., Csiki-Sava, Z., Andrei, R. A., Acheson, K. A., et al. (2016). A dinosaurian facial deformity and the first occurrence of ameloblastoma in the fossil record. Sci. Rep. 6:29271. doi: 10.1038/srep29271
- Brookes, P. (1990). The early history of the biological alkylating agents, 1918–1968. Mutat. Res. 233, 3–14.
- Farber, S., Diamond, L. K., Mercer, R. D., Sylvester, R. F., and Wolff, J. A. (1948). Temporary remissions in acute leukemia in children produced by folic antagonist, 4-aminopteroylglutamic acid (aminopterin). N. Engl. J. Med. 238, 787–793.
- Imbert, T. F. (1998). Discovery of podophyllotoxins. Biochimie 80, 207–222.
- Rothenberg, M. L. (1996). The current status of irinotecan (CPT-11) in the United States. Ann. N. Y. Acad. Sci. 803, 272–281.
- Weiss, R. B. (1992). The anthracyclines: will we ever find a better doxorubicin? Semin. Oncol. 19, 670–686.
- Nadler, L. M., Stashenko, P., Hardy, R., Kaplan, W. D., Button, L. N., Kufe, D. W., et al. (1980). Serotherapy of a patient with a monoclonal antibody directed against a human lymphoma-associated antigen. Cancer Res. 40, 3147–3154.
- Haanen, J. B., and Robert, C. (2015). Immune checkpoint inhibitors. Prog. Tumor Res. 42, 55–66. doi: 10.1159/000437178
- Seidel, J. A., Otsuka, A., and Kabashima, K. (2018). Anti-PD-1 and Anti-CTLA-4 therapies in cancer: mechanisms of action, efficacy, and limitations. Front. Oncol. 8:86. doi: 10.3389/fonc.2018.00086
- Falzone L, Salomone S, Libra M. Evolution of Cancer Pharmacological Treatments at the Turn of the Third Millennium. Front Pharmacol. 2018 Nov 13;9:1300. doi: 10.3389/fphar.2018.01300.